Разработка экспрессных, точных и чувствительных вариантов определения биологически активных соединений – одна из актуальных задач современной аналитической химии. Исследования в этой области стимулируются потребностями медицины, пищевой промышленности, ветеринарии, необходимостью мониторинга окружающей среды [1].
Определение высоко- и низкомолекулярных биологически активных соединений представляет как практический, так и теоретический интерес для изучения их свойств, содержания в сыворотке крови и других матриксах, влияния на организм человека и животных, структуры синтезированных соединений и биохимических реакций с их участием. Биологически активные соединения, как и многие физиологически активные вещества, способны оказывать положительное или отрицательное воздействие на организм в зависимости от дозы и длительности воздействия. Кроме того, в связи с широким применением высокоэффективных биологически активных соединений в других областях жизнедеятельности (например, в сельском хозяйстве) в воде и пищевых продуктах могут содержаться остатки этих препаратов в количествах, превышающих безопасный уровень. В связи с требованиями повышения качества жизни и увеличением поступлений фальсифицированной продукции на фармацевтический рынок, в последнее время необходимы разнообразные варианты количественного определения широкого круга биологически активных соединений, для оценки их качества, а также для определения их содержания в организме человека и животных [2].
Новейшие достижения в области создания био- и иммуносенсоров связаны с разработкой и получением новых функциональных материалов для физического трансдьюсера. Развиваются методы хемо- и биоселективного распознавания и связывания, а также эффективные методы микро- и наноструктурирования. Для электрохимических детекторов перспективным материалом являются тонкие пленки [3].
Среди тонких пленок в настоящее время особый интерес проявляется к проводящим пленкам Ленгмюра-Блоджетт на основе квазиодномерных комплексов с переносом заряда. Высокая проводимость пленок Ленгмюра-Блоджетт – необходимое условие их использования в качестве материалов в тонкопленочных структурах биосенсорных устройств [1].
В связи со всем вышесказанным настоящие исследования направлены на конструирование полипептидных монослоев с ориентированными α-спиралями, главным образом, с применением поверхностной графт-сополимеризации и техники Лэнгмюра-Блоджетт. Метод Лэнгмюра-Блоджетт позволяет получать монослой молекул на поверхности раздела фаз воздух-жидкость и жидкость-жидкость перед переходом на твердый субстрат.
При выполнении работы использовали общепринятые, стандартные и оригинальные методы исследования биохимического и физико-химического анализа с использованием последних достижений науки и техники. Учет и обработку результатов проводили методами статистического и регрессионного анализа.
Термогравиметрический анализ
Термогравиметрический анализ проводили с использованием термогравиметрического анализатора Перкина-Эльмера при скорости нагревания 10°С/мин в атмосфере азота. Соотношение длин блоков (tBuLG)m-b-(MLGSLG)n определяется по формуле:
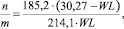
с потерями массы на первом этапе WL, вызванных выделением изобутилена, начинающихся при 180°С и заканчивающихся при 250 °С.
Элементный анализ
Элементный анализ осуществляли на анализаторе HEKAtech Gmbh Euro-EA CHN. Соотношение длин блоков сополимера можно рассчитать по формуле:
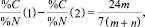
(1): (tBuLG)m-b-(MLGSLG)n, (2): (LGA)m-b-(MLGSLG)n – после удаления трет-бутильной защитной группы TFA.
ИК-спектроскопия нарушенного полного внутреннего отражения с Фурье- преобразованием
ИК-спектроскопию нарушенного полного внутреннего отражения с Фурье-преобразованием осуществляли на спектрофотометре Bruker IFS88 FT-IR при разрешении 4 см–1.
ИК-Фурье спектроскопия. ИК-Фурье спектроскопию на двусторонних полированных силиконовых субстратах осуществляли при разрешении 3 см-1 под вакуумом на спектрофотометре Bruker IFS66 V/S FT-IR.
В настоящем исследовании ставилась цель получить монослои с однонаправлено выровненными a-спиралями поли(γ-метил-L-глутамат-транс-γ-стерил-L-глутамата) с содержанием стерильного компонента 30 мол. % (ПMLГСLГ). Гидрофобное соединение ПMLГСLГ с жесткой структурой позволяет получить прочные пленки Лэнгмюра-Блоджетт с высоко ориентированными a-спиралями, расположенными параллельно субстрату, с гибкими стерил-цепочками. Полиглутаматы проявляют лиотропные и термотропные свойства и получили широкое распространение в последние годы.
На рис. 1 представлены π-А-изотермы для (LГК)63-β-(MLГСLГ)39 и (LГК)59-β (MLГСLГ)82, находящихся на поверхности воды при 20 °С в сравнении с изотермами для ПLГК и ПMLГСLГ. Изотерма ПLГК, находящейся на поверхности чистой воды, похожа на изотерму, опубликованную для натриевой соли ПLГК при рН 3,0. ПLГК – это в некоторой степени активная поверхность, проявляющая переход при низком поверхностном давлении 5–7 мN/м. Как известно из литературных данных, изотерма ПMLГСLГ имеет крутой подъем давления вследствие упаковки a-спиралей на поверхности за счет жидко-конденсированной фазы. При последующем сжатии монослоя ПMLГСLГ наблюдается коллапс с переходом на плато при 33 мN/м. Изотермы диблок сополимеров ПLГК-β-ПMLГСLГ проявляют совершенно другое поведение. При сжатии сначала наблюдается переход, аналогичный изотерме ПLГК при тех же самых условиях детектирования, а затем происходит линейное увеличение поверхностного давления. Для (LГК)59-β (MLГСLГ)82 с более длинным гидрофобным блоком наблюдается другой переход выше 40 мN/м.
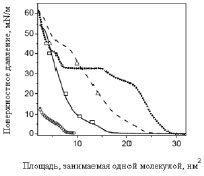
Рис. 1. π-А-изотерма (LГК)63-β-(MLГСLГ)39 (сплошная линия), (LГК)59-β (MLГСLГ)82 (сплющенная линия), (MLГСLГ)118 (пунктирная линия) и (LГК)63 (открытые циклы) на водной поверхности при 20 °С
На рис. 2 представлены кривые стабилизации (LГК)63-β-(MLГСLГ)39 и (LГК)59-β (MLГСLГ)82, полученные при различных величинах поверхностного давления. Устойчивые, трансферабельные монослои были получены с отношением переходов около единицы во всем диапазоне поверхностных давлений.
Как следует из точек стабилизации, представленных на рис. 2, площади, занимаемые молекулами, в которых монослои стабилизируются в соответствии с π-A-изотермой, что свидетельствует об отсутствии эффектов релаксации. Только выше второго перехода на изотерме, записанной для (LГК)59-β (MLГСLГ)82, т.е. при 45 мN/м, точка стабилизации сдвигается в область низких площадей. Это подразумевает, что переход, который может быть связан с перераспределениями цепей, является более медленным процессом. Хотя монослои стабилизируются при 45 мN/м, сдвиг пленки приводит к частичному переходу. Возможно, поэтому монослой в этом состоянии является неподвижным.
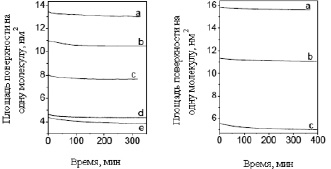
а б
Рис. 2. а – кривые стабилизации (LГК)63-β-(MLГСLГ)39 при 6 (а), 9 (b), 20 (с), 40 (d) и 45 (е) мN/м; б – кривые стабилизации (LГК)59-β (MLГСLГ)82 при 20 (а), 35 (b) и 45 (с) мN/м
Результаты угловой микроскопии Брюстера получали в процессе сжатия-расширения на чистой водной поверхности при различных значениях рН субфазы (рис. 3–5). При распределении по чистой водной поверхности образуется монослойная область с водными промежутками. Давление уменьшает водные промежутки, и, как только возникает поверхностное давление, образуется гомогенный монослой. Для обоих ПLГК-β-ПMLГСLГ при величине давления 45–50 мN/м не зарегистрирован монослойный коллапс. При расширении монослой сначала разрушается, а затем возвращается в исходное состояние.
Сообщалось для поли (γ-бензил-L-глутамата) (ПБLГ) молекулы без внешнего давления агрегируются в 2D-островки толщиной в одну молекулу на водной поверхности. По сравнению с PBLG, на чистой водной поверхности (LГК)63-β-(MLГСLГ)39 образует намного более мелкие агрегаты (рис. 3). Это, вероятно, связано, с взаимодействиями между длинными гидрофильными блоками ПLГК и водной поверхностью, что ограничивает множественные антипараллельные связи между молекулами. Таким образом, при увеличении активной поверхности диблок сополимеров либо снижением рН субфазы, либо повышением DPPMLGSLG, образуется более агрегированный монослой (рис. 4 а, b, 5). Напротив, при высоком значении рН 8,6, когда ПLГК полностью заряжен, агрегации не наблюдается (рис. 4, с, d). Водная солюбилизация ПLГК при этом рН приводит к молекулярной реориентации, препятствуя антипараллельным ориентациям спиралей.
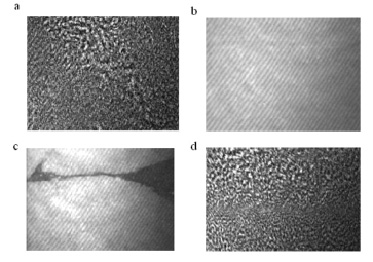
Рис. 3. Результаты угловой микроскопии Брюстера (420×522 мкм) (LГК)63-β-(MLГСLГ)39 при сжатии до 45 мN/м на чистой водной поверхности при 20°С, полученные при А = 32 (а) и 17 (b) нм2/молекула. При соответствующем расширении изображения получали при А = 17 (а) и 32 (b) нм2/молекула

Рис. 4. Результаты угловой микроскопии Брюстера (420×522 мкм) (LГК)63-β-(MLГСLГ)39 при сжатии до 45 мN/м на чистой водной поверхности при 20°С, рН субфазы 2, полученные при А = 32 (а) и 25 (b) нм2/молекула. При рН 8,6 изображения получены при А = 30 (а) и 12 (b) нм2/молекула во время сжатия

Рис. 5. Результаты угловой микроскопии Брюстера (420×522 мкм) (LГК)59-β (MLГСLГ)82 при сжатии до 50 мN/м на чистой водной поверхности при 20°С, полученные при А = 39 (а) и 27 (b) и 23 (с) нм2/молекула. При соответствующем расширении изображения получали при А = 29 (d) нм2/молекула
Методом атомной силовой микроскопии показано, что получены гомогенные и однородные пленки Лэнгмюра-Блоджетт. На рис. 6 представлены типичные спектры, скорректированные с учетом линейного дихроизма, зарегистрированные в разных направлениях спектрополяриметра, для многослойных пленок Лэнгмюра-Блоджетт ПLГК-β-ПMLГСLГ. Эффект Лэнгмюра-Блоджетт вызван предпочтительной ориентацией α-спиралей вдоль поверхности погружения. Скорректированные спектры анализировали в различных направлениях, сопоставляя друг с другом. В результате показано, что наблюдается один максимум при 191 нм и два минимума при 208 и 222 нм. Это свидетельствует о том, что полученные пленки ПLГК-β-ПMLГСLГ имеют правостороннюю α-спиральную структуру.
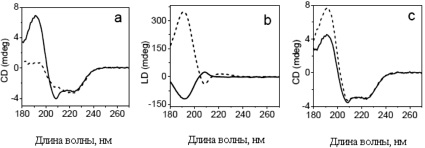
Рис. 6. CD-спектры, LD- спектры и скорректированные CD-спектры многослойной пленки Лэнгмюра-Блоджетт (LГК)63-β-(MLГСLГ)39, записанные при 40 мN/м. Образец анализировался в двух разных направлениях: горизонтальном (сплошная линия) и вертикальном (пунктирная линия)
На рис. 7 представлены ИК-спектры монослоев Лэнгмюра-Блоджетт (LГК)63-β-(MLГСLГ)39, полученные на чистой воде при различных значениях рН. При рН субфазы 8,6 протяженная связь С = О водородной связи карбоксильной группы при 1711 см–1 исчезает, и появляется полоса ионизованной карбоксильной группы при 1560 см–1, свидетельствуя о том, что происходят изменения α-структуры в блоке ПLГК. Спектры монослоев, приготовленных на чистой воде при рН субфазы 2, идентичны друг другу, проявляя характеристические полосы амида I и амида II при 1653 и 1548 см–1. Отсюда следует, что, даже когда ПLГК-β-ПMLГСLГ расположен на поверхности чистой воды, преобладающей является α-структура.
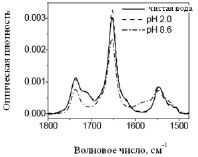
Рис. 7. ИК-спектр монослоев Лэнгмюра-Блоджетт (с обеих сторон силиконового субстрата) (LГК)63-β-(MLГСLГ)39, записанный при 40 мN/м
Известно, что ПLГК образует полностью α-спиральную структуру в водных растворах при рН ниже 5,0. Его переход между α-спиральной и случайной конформациями происходит в области рН от 5,0 до 6,0, где содержание α-структуры составляет 80–70 %. Преобладающая α-спиральная структура монослоя ПLГК-β-ПMLГСLГ на поверхности чистой воды частично является следствием того, что поверхность воды имеет более кислое значение рН (около 5,5), увеличиваясь при повышении содержания атмосферного СО2, диссоциируемого в субфазе. Исследования α-спиральных переходов ПLГК в водных растворах, содержащих осмолиты, показали увеличение осмотического давления с преобладанием α-спиральных форм.
Таким образом, осмотическое давление внутри ПLГК может увеличивать стабильность α-спиральной структуры.
Работа выполнена в рамках федеральной целевой программы «Научные и научно-педагогические кадры инновационной России на 2009–2013 годы», государственный контракт № 16.512.11.2220.
Библиографическая ссылка
Бабич О.О., Солдатова Л.С., Разумникова И.С., Просеков А.Ю. ИСПОЛЬЗОВАНИЕ МЕТОДА ЛЕНГМЮРА-БЛОДЖЕТТ ДЛЯ ПОЛУЧЕНИЯ ПЛЕНОК С ЦЕЛЬЮ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ // Успехи современного естествознания. – 2013. – № 6. – С. 73-78;URL: https://natural-sciences.ru/ru/article/view?id=32484 (дата обращения: 19.04.2024).



